Toxina botulínica y espasticidad
AUTOR: FRCA. ROSARIO GONZALEZ NUÑEZ fisioterapeuta
centro de trabajo asociacion de esclerosis multiple de zamora
kampanilla2002@hotmail.com
centro de trabajo asociacion de esclerosis multiple de zamora
kampanilla2002@hotmail.com
INDICE
1-INTRODUCCIÓN
2- LA TOXINA BOTULÍNICA
3-LA TOXINA BOTULÍNICA Y LA TRANSMISIÓN DEL IMPULSO NERVIOSO
4-FARMACOCINÉTICA Y PRESENTACIÓN
5-EFECTOS SECUNDARIOS Y COTRAINDICACIONES
6-APLICACIONES
7-ESPASTICIDAD
8A- APLICACIÓN DE LA TOXINA EN LA ESPASTICIDAD
8B-PUNTOS DE MAYOR EFECTIVIDAD DE LA TOXINA BOTULÍNICA
3-LA TOXINA BOTULÍNICA Y LA TRANSMISIÓN DEL IMPULSO NERVIOSO
4-FARMACOCINÉTICA Y PRESENTACIÓN
5-EFECTOS SECUNDARIOS Y COTRAINDICACIONES
6-APLICACIONES
7-ESPASTICIDAD
8A- APLICACIÓN DE LA TOXINA EN LA ESPASTICIDAD
8B-PUNTOS DE MAYOR EFECTIVIDAD DE LA TOXINA BOTULÍNICA
La toxina botulínica tipo A se esta
convirtiendo en el tratamiento de elección ante multitud de patologías
relacionadas con alteraciones en la bioquímica de la acetilcolina.
Desde mediados del siglo XX se están realizando multitud de ensayos
de este tipo. La toxina botulínica A es la más utilizada en ensayos
terapéuticos en humanos; los mas destacados son:
- Ensayos terapéuticos realizados por Alan Scott ; en 1.973
este autor comenzó a utilizar toxina botulínica tipo A en el tratamiento
del estrabismo, al principio en primates no humanos y desde 1980 en
humanos. También describió su uso en la miopatía orbital endocrina y en
la parálisis del recto lateral.
• Ensayos terapéuticos realizados por Frueh et al que en
1.984 describieron el uso de la toxina A en el blefarospasmo; en los
años subsiguientes las inyecciones de toxina se transformaron en un
tratamiento de primera línea para el blefarospasmo con muy buenos
resultados (mejoría espectacular en más del 80% de pacientes inyectados)
• Ensayos terapéuticos realizados por Tsui et al (1.985) y por Brin et al
(1986); estos investigadores comunicaron los resultados de pruebas
terapéuticas abiertas con inyecciones de toxina A para la tortícolis en
pacientes que no habían respondido a otros tratamientos y que se
hallaban gravemente afectados.
• Ensayos terapéuticos realizados por Jan-kovic, Gelb y Greene
que entre los años 1.986 y 1.991 han realizado por lo menos cinco
estudios ciegos con control de placebo, centrandos en la toxina A para
las distonías cervicales. Más adelante, estudiaron su uso en la distonía
oro-mandibular, laríngea y de miembros confirmándose su utilidad
particularmente en el tratamiento de la distonía mandibular de cierre y
de la distonía laríngea en aducción.
La toxina botulínica representa la toxina biológica más potente de las conocidas hasta hoy.
Esta toxina es producida por una bacteria anaeróbica y Gran positiva, el Clostridium Botulinum
de la que se conocen hasta 8 tipos inmunológicamente distintos, pero
solo los tipos A, B y E se han vinculado al botulismo humano.
El Costridium Botulinum se halla ampliamente distribuido por la
naturaleza (en suelos, lodo de lagos o charcas y en la vegetación), por
lo que los contenidos intestinales de peces, pájaros y mamíferos pueden
contener este tipo de micro-organismo. Sus esporas son bastante
resistentes, en especial al calor (por eso para evitar su presencia en
los alimentos las industrias conserveras tienen que emplear métodos de
esterilización).
En la especie humana produce una enfermedad conocida como botulismo ,
que no es una enfermedad infecciosa propiamente dicha, sino una
intoxicación por ingestión de alimentos que contienen la toxina (es
decir no se debe a la multiplicación en el conducto gastro-intestinal de
esta bacteria).
Esta toxina es relativamente lábil al calor y es completamente
inactivada a 100º C durante unos 10 minutos. Sin embargo no es
inactivada ni por la acidez de las secreciones gástricas ni por las
enzimas proteolíticas del estómago y del duodeno.
Su toxicidad está relacionada con su afinidad para con las células
del sistema nervioso central. Se sabe que sus acciones farmacológicas
están relacionadas con el bloqueo de la liberación de acetilcolina en
las terminaciones desmielinizadas de los nervios motores colinérgicos.
Además los estudios electrofisiológicos han demostrado que bloquea la
liberación del transmisor de estas terminaciones.
El botulismo humano se produce generalmente entre las dieciocho y las
treinta y seis horas desde la ingestión del alimento contaminado,
siendo sus primeros síntomas, debilidad, vértigos, gran sequedad de la
orofaringe, nauseas y vómitos; poco después aparecen signos neurológicos
como alteraciones de la visión, dilatación pupilar, incapacidad para la
deglución, dificultad para hablar, retención urinaria, debilidad
generalizada de la musculatura esquelética y parálisis respiratoria.
Hasta hace no muchos años la mortalidad de esta enfermedad era
extraordinariamente elevada, pero en los últimos años se ha conseguido
reducirla hasta una cifra en torno a un veinte por ciento.
Afortunadamente son relativamente pocos los casos que se producen en el
hombre, siendo mucho mas frecuente en otras especies animales.
Se conocen diversos tipos de Clostridium Botilinum, cada uno de los
cuales produce una neurotoxina inmunologicamente distinta de las otras,
que como ya se ha comentado se hallan entre las mas potentes que existen
(un microgramo contiene doscientas mil veces la dosis letal mínima para
el ratón y es aproximadamente igual a la dosis letal para el hombre).
Los tipos A, B, E y F son los que con mas frecuencia producen el
botulismo humano mientras que los tipos C y D producen el botulismo en
las aves y en el ganado bovino respectivamente.
La producción de la toxina por la bacteria acompaña a la germinación
de las esporas y al crecimiento de las células vegetativas, de forma que
en los cultivos de Clostridium Botulinum toxigénico no hace su
aparición hasta que el crecimiento bacteriano ya esta avanzado y
comienza a producirse autolisis.
El tipo A que es el que interesa en farmacología humana forma un
complejo con la hemaglutinina, que ha podido ser cristalizado; se trata
de una proteína de peso molecular 900.000daltons. La separación de la
hemaglutinina puede llevarse a cabo sin que la toxina pierda efectividad
y posee una fracción neurotóxica constituida por una proteína con un
peso molecular de aproximadamente 150.000 daltons (se sospecha que esta
formada por subunidades tóxicas de menor tamaño).
La neurona tiene dos funciones principales, la propagación del
potencial de acción (impulso nervioso) a través del axón y su
transmisión a otras neuronas o a las células efectoras (músculo
esquelético, músculo cardíaco, las glándulas exocrinas y glándulas
endocrinas reguladas por el sistema nervioso) para inducir una
respuesta.
La conducción de un impulso a través del axón es un fenómeno
eléctrico causado por el intercambio de iones Na + y K + a lo largo de
la membrana. La trasmisión del impulso de una neurona a otra o a una
célula efectora depende de la acción de neurotransmisores específicos
sobre receptores también específicos.
Una neurona determinada recibe gran cantidad de estímulos de forma
simultánea, positivos y negativos, de otras neuronas y los integra en
varios patrones de impulsos diferentes. Éstos viajan a través del axón
hasta la siguiente sinapsis.
Una vez iniciada la propagación axonal del impulso nervioso, ciertas
drogas o toxinas pueden modificar la cantidad de neurotransmisor
liberada por el axón terminal; precisamente esta el la forma de la que actúa la toxina botulínica : bloqueando la liberación de acetilcolina .
Las sinapsis se establecen entre neuronas y en la periferia entre una
neurona y un efector (músculo, etc.). La conexión funcional entre dos
neuronas puede establecerse entre el axón y el cuerpo celular, entre el
axón y la dendrita (la zona receptiva de la neurona), entre un cuerpo
celular y otro o entre una dendrita y otra.
El cuerpo neuronal produce ciertas enzimas que están implicadas en la
síntesis de la mayoría de los neurotransmisores. Estas enzimas actúan
sobre moléculas precursoras captadas por la neurona para formar el
correspondiente neurotransmisor. Éste se almacena en la terminación
nerviosa dentro de vesículas.
Cuando un potencial de acción alcanza la terminación activa una
corriente de calcio y precipita simultáneamente la liberación del
neurotransmisor desde las vesículas por la fusión de la membrana de las
mismas a la de la terminación neuronal. Así las moléculas del
neurotransmisor son expulsadas a la hendidura sináptica por exocitosis.
La cantidad de neurotransmisor en las terminaciones se mantiene
relativamente constante e independiente de la actividad nerviosa
mediante una regulación estrecha de su síntesis.
Los neurotransmisores difunden a través de la hendidura sináptica, se
unen inmediatamente a sus receptores y los activan induciendo una
respuesta fisiológica. Dependiendo del receptor, la respuesta puede ser
excitatoria (iniciando un nuevo potencial de acción) o inhibitoria
(frenando el desarrollo de un nuevo potencial de acción).
La interacción neurotrnasmisor-receptor debe concluir también de
forma inmediata para que el mismo receptor pueda ser activado
repetidamente. Para ello será captado rápidamente por la terminación
postsináptica mediante un proceso activo de recaptación y destruido por
enzimas próximas a los receptores, o bien difunde en la zona adyacente.
De entre todos los neurotransmisores nos interesa recordar que la acetilcolina
es el neurotransmisor fundamental de las neuronas motoras
bulbo-espinales, de las fibras preganglionares autónomas, las fibras
colinérgicas posganglionares (parasimpáticas) y muchos grupos neuronales
del sistema nervioso central (como los ganglios basales y la corteza
motora).
Se sintetiza a partir de la colina y la acetil-coenzima A
mitocondrial, mediante la colin-acetil-transferasa y al ser liberada
estimula receptores colinérgicos específicos; su interacción finaliza
rápidamente por hidrólisis local a colina y acetato mediante la acción
de la acetil-colinesterasa. Los niveles de acetilcolina están regulados
por la colin-acetil-transferasa y el grado de captación de colina.
La toxina Botulínica es precisamente una sustancia anticolinérgica, ya que actúa como relajante muscular e inhibidora específica de la liberación de acetilcolina ;
en efecto, actúa sobre la terminación nerviosa presináptica impidiendo
la acción de los iones de calcio en el proceso de exocitosis necesario
para la liberación de acetilcolina, disminuyendo de esta forma el
potencial de placa y causando una parálisis muscular.
La toxina tiene dos subunidades, una de las cuales se une al receptor
de membrana responsable de la especificidad, permitiendo la entrada de
la otra subunidad que es la que produce el bloqueo de los iones calcio.
Cuando se emplea en terapéutica, por su forma de administración solo
interfiere la trasmisión neuromuscular en el lugar de la aplicación y la
recuperación del impulso nervioso tiene lugar gradualmente a medida que
las terminaciones nerviosas se van regenerando, proceso que dura de
seis a ocho semanas en los animales de experimentación.
Como ya hemos indicado la toxina botulínica del tipo A
es la más ampliamente empleada en ensayos terapéuticos en humanos,
aunque se han estudiado otras como la toxina botulínica del tipo F cuya
utilidad esta limitada por la corta duración de su efecto y la toxina
botulínica del tipo B que está siendo valorada en la actualidad en
pruebas clínicas.
En cualquier caso la toxina botulínica produce parálisis muscular a
través de su unión irreversible con el terminal nervioso colinérgico
presináptico, donde al integrase causa la disrupción del flujo del
calcio iónico.
Dicho mecanismo de actuación interfiere en la liberación de la acetilcolina intravesicular. El resultado es una denervación funcional transitoria que causa parálisis, atrofia muscular y anomalías electromiográficas.
Como ya hemos avanzado la toxina posee dos subunidades, de forma que
una de ellas se une al receptor de membrana permitiendo la entrada de la
segunda subunidad dentro de la célula donde va a ejercer un efecto
tóxico inactivando enzimas específicas; ello involucra una reacción de
ADP-riboxilación (se cree que la toxina inactiva de esta forma a la
actina) y se admite que hacen falta solo unas pocas moléculas para
inhibir la liberación de la acetilcolina.
La debilidad muscular causada por esta toxina se mantiene restringida al área inyectada ,
existiendo evidencias histológicas de que se produce una toxicidad
restringida a las fibras musculares extrafusales, mientras que las
fibras intrafusales quedan relativamente exentas de esta afectación.
Ello causa una alteración en la relación de las neuronas motoras alfa
y gamma y en consecuencia se produce, no sólo una parálisis local, sino
también un efecto en los mecanismos de control motor central.
Con respecto a su forma de presentación ,
el único tipo de toxina botulínica disponible comercialmente es el tipo
A. En los Estados Unidos está comercializada por el laboratorio
californiano Allergan Pharmaceuticals con el nombre comercial “botox”.
Se presenta en una preparación liofilizada y secada al frío. Se trata
de ampollas que deben guardarse congeladas a –5° C, de tal modo que la
toxina se reconstituye en el momento de la inyección con suero
fisiológico salino estéril (sin preservativo).
Su potencia se expresa en unidades, de tal manera que una unidad es
equivalente a la cantidad de toxina capaz de matar al 50% de un grupo de
ratones hembras Swiss-Webster de entre 18 y 20 gramos de peso (DL50).
En los Estados Unidos, aproximadamente 0,4 nanogramos de la toxina
proteica equivalen a 1 unidad (o expresado de otra forma 2,5 unidades
son equivalentes a 1 nanogramo).
En el caso de la toxina botulínica tipo A europea, conocida
comercialmente como “dysport”, la potencia del preparado es diferente ya
que 1 nanogramo equivale a 40 unidades.
Debido a esta divergencia de potencia en los preparados comerciales
de toxina botulínica, no es rara la utilización de dosis superiores a
500 unidades por sesión con la preparación europea.
La dosis letal de la toxina botulínca americana tipo A (botox)
inyectada en monos jóvenes es aproximadamente de 40 unidades por
kilogramo de peso que, cuando es extrapolada, representa alrededor de 50
veces la dosis promedio inyectada para el tratamiento de la distonía
focal.
La DL50 estimada en humanos es de 2.500-5.000 unidades según algunos autores y más cercana a 5.000 de acuerdo con otros.
La solución diluida se recoge en una jeringa de tuberculina y la
toxina se inyecta con una aguja de un calibre de 26 a 30 y de 0,5
pulgadas de largo en los músculos superficiales y de calibre 22 con 1,5
pulgadas de largo en los músculos profundos.
Se pueden preparar diferentes diluciones dependiendo del sitio que va
ha ser inyectado, como por ejemplo, 2,5-5 unidades por 0,1 cc para
músculos cervicales y 1,25-2,5 unidades por 0,1 cc para un blefarospasmo
o para un espasmo hemifacial.
El tiempo preciso para que aparezca su acción oscila entre dos y tres
días, alcanzando su efecto máximo cinco o seis días después de la
inyección, durando su efecto un periodo variable que se extiende desde
las dos semanas hasta los ocho meses (aunque hemos encontrado algunos
estudios que señalan que esta duración puede extenderse hasta los once
meses), que es el tiempo necesario para el proceso de unión de la
toxina, integración de la misma y regeneración de la unión neuromuscular
.
Como ya hemos avanzado la toxina posee dos subunidades, de forma que
una se une al receptor de membrana permitiendo la entrada de la segunda
subunidad dentro de la célula donde va a ejercer un efecto tóxico
inactivando enzimas específicas, para ello involucra una reacción de
ADP-riboxilación (se cree que la toxina inactiva de esta forma a la
actina). Se piensa que hacen falta solo unas pocas moléculas para
inhibir la liberación de la acetilcolina.
Se ha observado como la administración de la toxina botulínica puede
dar lugar en ocasiones a algunos efectos sistémicos que son generalmente
leves pero que deben ser tenidos en cuenta. Son principalmente los
siguientes:
• Defecto en la neurotransmisión a distanca , que suele ser reversible y subclínico (con técnicas de electomiografía de fibra única se ha objetivado un aumento del “jitter”
en puntos distantes al lugar de aplicación; estas alteraciones son
reversibles con mejoría en unos dos o tres meses, y no tiene traducción
clínica ya que no aparece debilidad).
• Aparición de anticuerpos antitoxina botulínica ; se han
detectado anticuerpos en pacientes tratados con toxina botulínica,
principalmente en casos de distonía cervical, aunque también con
blefaroespasmo. La incidencia de aparición de estos anticuerpos según
los diferentes autores se sitúa entre un 3 y un 57%. Esta variabilidad
está causada muy probablemente por las diferentes técnicas empleadas en
la detección. Los anticuerpos antitoxina botulínica aparecen con más
frecuencia en aquellos pacientes que han recibido aplicaciones mas
repetitivas, dosis mas altas o aplicaciones suplementarias. No parece
tener relación con la edad del paciente, la duración del tratamiento, el
número de aplicaciones o la dosis total acumulada. Con los datos
disponibles actualmente no se podido correlacionar la presencia de este
tipo de anticuerpos con la aparición de resistencia al tratamiento
(aunque se postula que en algún caso se podría justificar la pérdida de
eficacia de la toxina por esta causa, de modo que estaría indicada la
toxina botulínica F que produce respuestas equiparables pero de solo
alrededor de un mes de duración).
• Fatiga generaliza con leve debilidad y síntomas “ flu-like ”
(nauseas, somnolencia, cefalea, malestar general, etc.); la valoración
electrodiagnóstica es normal lo que indica que estos síntomas no son
debidos al efecto de la toxina botulínica en la transmisión
neuromuscular.
• Los pacientes también pueden desarrollar signos de disfunción autonómica ;
así en pacientes con tortícolis se puede producir una parálisis de la
musculatura lisa de los conductos salivales produciendo sequedad en la
boca.
• Así mismo, se han demostrado alteraciones leves en los reflejos cardiovasculares .
Con respecto a las contraindicaciones del uso de la toxina botulínica, deben ser señaladas las siguientes:
• Pacientes alérgicos al medicamento
• Trastornos generalizados de la función muscular (como por ejemplo la miastenia gravis).
• Tomar anticoagulantes
• Inflamación o infección en el punto de inyección
• Administración de dosis elevadas de antibióticos aminoglucosidos (sobre todo en pacientes con insuficiencia renal)
• Embarazo
• Falsa expectativa de curación
• Inseguridad de un seguimiento terapeútico
Con respecto a las precauciones que deben tenerse para el empleo de estos preparados, hay que indicar las siguientes:
• Debe tenerse gran precaución en pacientes con alteraciones
respiratorias durante el tratamiento de la tortícolis debido al riesgo
de aspiración.
• Durante el periodo de lactancia, no se sabe si es secretado en
cantidades significativas en la leche materna así que como precaución
debe evitarse su utilización en este periodo
| DISTONIA FOCAL | Blefaroespasmo típico Apraxia del párpado Distonía oromandibular-facial lingual Distonía cervical ( tortícolis ) Distonía laríngea ( disfonía espasmódica ) Calambre ocupacional Otras ( mano, pie.. .) |
| MOVIMIENTOS ANORMALES | Espasmo hemifacial Temblor ( cefálico, voz y extremida des) Mioclonus ( paladar, espinal ) Tics motores distónicos |
| CONTRACCIONES INAPROPIADAS | Espasticidad Contracturas lumbosacras Radiculopatía y espasmo muscular Tartamudeo Bruxismos y alteraciones de la ATM |
| EN LA MUSCULATURA LISA | Acalasia Disfunción del esfínter de Oddi Disinergia rectoesfinteriana Fisura anal crónica Vejiga espástica Otras alteraciones espasmódicas |
| INDICACIONES OFTALMOLÓGICAS | Estrabismo Nistagmus con oscilopsia Ptosis |
| OTRAS APLICACIONES | Cosmética Obesidad Sudoración excesiva Lagrimeo excesivo |
De todas ellas la que mayor repercusión ha tenido es su empleo en el tratamiento de las distonías focales ;
en estos casos su utilización ha significado una opción muy eficaz y un
cambio radical en el pronóstico y en la calidad de vida de los
enfermos, estando aceptada su utilización como tratamiento habitual.
En el siguiente cuadro se pueden apreciar de forma resumida los
porcentajes de eficacia, duración y complicaciones del empleo de esta
toxina en los diferentes tipos de distonia focal:
| DISTRIBUCION | MEJORA | INICIO | DURACIÓN | COMPLICACIONES |
Blefaroespasmo |
90 %
|
1-3 días
|
12-15 semanas
|
ptosis
|
| Oromandibular |
70 %
|
2-7 días
|
12-14 semanas
|
disfagia
|
| Cervical |
70 %
|
3-7 días
|
8-12 semanas
|
disfagia
|
| Laríngea aductora |
96 %
|
1-2 días
|
10-16 semanas
|
disfagia voz
|
| Laríngea abductora |
70 %
|
1-2 días
|
10-16 semanas
|
disfagia voz
|
| De la mano |
60-80 %
|
3-7 días
|
12-14 semanas
|
debilidad mano
|
La más significativa de todas las distonías focales que se ha tratado con la toxina botulínica es el blefaroespasmo .
Existen muchas definiciones entre ellas vamos a resaltar la de la O.M.S . define espasticidad como como la resistencia dependiente de la velocidad contra un movimiento pasivo; Lance
(1982) la define como la reorganización plástica del sistema nervioso
central en una situación de déficit de controles inhibitorios, Wiesendanger
(1991) como un trastorno locomotor, que se desarrolla de forma gradual
como respuesta a una pérdida parcial o total del control supraespinal
sobre la médula espinal caracterizada por la modificación de los
patrones de activación de las unidades motoras que reaccionan ante
señales sensoriales y centrales llevando a contracciones concomitantes,
patrones totales y patrones anormales, Bettina Paeth como la activación
descoordinada de moléculas actina-miosina tanto intra como
intermuscularmente que provocan una contracción de los filamentos
musculares (un acortamiento muscular), que impide la contracción
excéntrica y el desarrollo de una fuerza adaptada. También puede ser
definida como la hipertonía debida a la lesión de las fibras piramidales estrictas
o corticoespinales directas, asociada a la de otros sistemas de fibras
que discurren en intima asociación con ellas, constituye una forma de
disminución de la pasividad neuromuscular que suele acompañarse de
exaltación de los reflejos musculares clínicos y a veces del fenómeno de
la “navaja de muelle.

La espasticidad puede aparecer en muy diversas situaciones clínicas, siendo las más importantes, en función de su frecuencia las parálisis cerebrales infantiles (PCI), seguidas de lejos por los accidentes cerebro-vasculares (ACV), la esclerosis múltiple (EM), los tumores y otras, tal y como se muestra en el gráfico.
Topográficamente hablando afecta preferentemente a los miembros
inferiores siendo los músculos implicados los flexores, aductores y
rotadores internos, consecuencia de la afectación de la primera
motoneurona encontramos paresia, hiperreflexia y reflejos plantares
flexores
El objetivo perseguido al aplicar la toxina sobre el músculo son:
-Disminuir gradualmente el potencial de la placa motriz
-Disminuir el estado de hipercontracción
-La relajación muscular
-Facilitar la extensibilidad
-EN el caso de niños facilitar el crecimiento longitudinal del músculo
-Una mejora de la función, tras la aplicación en los miembros
inferiores encontraremos: una mejora de la marcha en la que observaremos
mayor comodidad, equilibrio y una disminución de las caídas, si la
aplicación es en el miembro superior nos encontraremos con una mayor
facilidad para la realización de las actividades de la vida diaria
(higiene, comida, etc)
-Prevenir complicaciones a largo plazo: luxaciones, deformidades osteoarticulares principalmente de cadera, pie y muñeca.
-Mejorar la circulación sanguínea
-Favorece la colocación de ortesis y calzado
-Disminuye el dolor asociado a la postura mantenida
-Una mejora estética
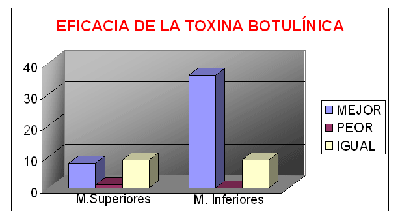
los principales puntos de infiltración en el miembro inferior son: triceps, tibial posterior, tibial anterior, abductor del dedo gordo, abductores y psoas, la principal aplicación ha sido empleada sobre todo en la espasticidad abductora de las piernas, consiguiéndose una reducción de la espasticidad, del dolor y una mejoría de la higiene y cuidado del enfermo . También se ha empleado en la espasticidad en extensión de las piernas (pie caído espástico) aplicándola a los músculos sóleos, tibial posterior y gemelos, objetivándose una mejoría en el tono muscular, en la marcha y en el dolor del pie con reducción del clonus aquíleo, en la displasia de cadera (provocada por el psoas) y de especial interese porque puede llegar a ser luxante Por último también se ha demostrado su utilidad en la espasticidad de extremidades superiores, debiendo señalarse que en general son mejores los resultados en personas jóvenes, en las que las articulaciones son más dinámicas.
 Aunque la utilización de la toxina botulínica es muy eficaz para la
corrección de retracciones, como es le caso de la del tendón de Aquiles,
debe tenerse en cuenta antes de decir su aplicación que no es
igualmente eficaz en los miembros superiores que en los inferiores, como
puede verse en el gráfico anterior
Aunque la utilización de la toxina botulínica es muy eficaz para la
corrección de retracciones, como es le caso de la del tendón de Aquiles,
debe tenerse en cuenta antes de decir su aplicación que no es
igualmente eficaz en los miembros superiores que en los inferiores, como
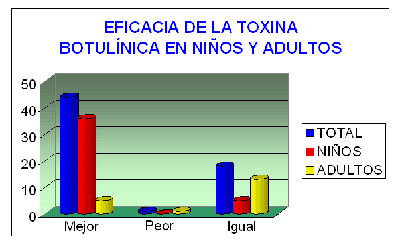
puede verse en el gráfico anterior El empleo de la toxina botulínica es especialmente interesante y útil en los niños con parálisis cerebral espástica . Es sin lugar a dudas un agente muy efectivo, tal y como puede apreciarse en la siguiente gráfica, donde se comparan los resultados obtenidos con este tipo de tratamiento en niños y adultos.
Gracias a la aplicación precoz de la toxina botulínica en estos niños
con parálisis cerebral espástica podemos prevenir las contracturas y
reducir el número de intervenciones quirúrgicas a las que habrá que
someterles.
En el inicio de los años noventa el tratamiento de estos niños se
centraba en la fisioterapia, férulas, estimulación eléctrica, etc.
(terapia física) y en el uso de medicamentos antiespásticos orales; los
efectos así obtenidos eran breves y terminaban por perderse. Sin
embargo, desde que se empezó a utilizar la toxina botulínica, la meta
principal se ha convertido en debilitar selectivamente los músculos
responsables de la contracción espástica.
Se recomienda el tratamiento precoz con toxina botulínica, a ser
posible antes de los seis años para evitar el desarrollo de contracturas
fijas, prevenir luxaciones (especialmente las de cadera) y posponer o
eliminar la necesidad de recurrir a la cirugía correctora.
En cuanto al modo de administrar la toxina, tras realizar diferentes
estudios parece ser que se ha llegado a la conclusión de que no existe
diferencia entre inyectar cerca del punto motor o en el vientre
muscular.
Parece probable que cada músculo tenga respuesta a una dosis optima y
que las inyecciones de cantidades desproporcionadamente altas de toxina
en un solo músculo sean inadecuadas. En su lugar, la toxina debe ser
distribuida en varios músculos de acuerdo a su contribución en el cuadro
clínico.
Los efectos secundarios producidos por este tratamiento de la
espasticidad son considerados menores y están caracterizados por la
aparición de debilidad (en los músculos inyectados y no inyectados),
paresia transitoria de vejiga (después del tratamiento de la
espasticidad de los adductores de la cadera) y, en un número muy pequeño
de pacientes, un síndrome generalizado con tetraparesia (tipo
botulismo) que se presenta tras la inyección intramuscular de toxina
botulínica y desaparece en un periodo de unas cuatro semanas.
•
MANO ESCARVADA DE GARCIN: (Flexión de muñeca con desviación
cubital, adducción del pulgar y pronación). Los puntos de infiltración
los encontramos en el bíceps braquial, braquial anterior, cubital
anterior, palmares, flexores de dedos (sobre todo los superficiales)
• INCLUSIÓN DEL PULGAR: Adductor del pulgar en su cara posterior
porque la infiltración en su cara anterior resulta muy dolorosa por la
presencia de muchos receptores sensitivos,
• PATRON EN CANDELABRO: los puntos de infiltración se encuentran en
el flexor común de los dedos en el pronador cuadrado y redondo, en el
cubital posterior, supinador largo (su componente flexor), braquial
anterior y bíceps braquial.
• TRIPLE FLEXIÓN
• Flexión de cadera: infiltrar en recto anterior, sartorio, tensor
de la fascia lata, psoas iliaco, pectíneo, adductores, glúteo menor y
fibras anteriores del glúteo medio
• Flexión de rodilla: isquiotibiales, tensor de la fascía lata, gemelos y poplíteo.
• Flexión plantar (equino): tríceps, tibial posterior, flexor largo de los dedos.
• PATRÓN EN TIJERA:
• Adducción de cadera : pectíneo, aductores, recto interno
• Rotación interna: adductores.
• PIE EQUINO-VARO: tibial posterior, tríceps, musculatura intrínseca del pie.
• PIE VALGO: peróneo lateral largo y corto
BIBLIOGRAFÍA CONSULTADA :
- Aguilar-Barberá M., Calopa-Garriga M., Sánchez-Dalmau B. Indicaciones actuales del tratamiento con toxina botulínica . Rev. Neurol. 25: 138-270, 1.997.
- Callejas Pérez M.A., Rubio M., Grimalt R., Valls-Solé J. La hiprehidrosis primaria . Med. Integral; 36: 223-230; Marzo 1.996.
- Durif F . Clinical bioequivalence of the current comercial
preparations of botulinum toxin . En 2º Simposio Europeo sobre toxina
botulínica. Cannes. Marzo 1.995.
- Davis B.D., Dulbecco R., Eisen h. N., et al . Tratado de Microbiología . 2ª edición. Ed. Salvat. Barcelona, 1.979.
- Elston J.S. Botulinic toxin A in clinical medicine . J. Physiol (París); 285-289; 1.990.
- Hesse S., Lucke D. y Malezic M. Botulinum treatment for
lower limb extensor espasticity in chronic hemiparetic patients . J.
Neurol. Neurosurg. Psychiatry. 57:1.321-1.324; 1.994.
- Jankovic J., Brin M.F . Thrapeutic usus of botulin toxin . En N. Eng. J. Med.; 324:1186-1194. 1.991.
- Lehninger A.L., Nelson D.L. y Cox M.M . Principios de bioquímica . 2ª edición. Ed. Omega. Barcelona, 1.995.
- Sanders D.B., Nassey E.W., Buckley E.G. Botulinum toxin for blepharospasm: single fiber EMG studies . Neurology. 36:545-547;1.986.
- Snow B.J., Tsui J.K.C., Bharr M.H. et al. Treatment of spasticity with botulinum toxin: a double-blind study . Ann. Neurol.; 28: 512-515;1.990
- Valls-Solé J., Tolosa E.S., Martí M.J ., Allam N. Treatment
with botulinum toxin injections does not change brainstem inter-neural
escitability in patients with cervical dystonia . Clin. Neuropharmacol.
17-229; 1.994.
- VV.AA., Diccionario terminológico de Ciencias Médicas 13ª edición. Ed. Masson. Barcelona 1.996.
DIRECCIONES DE INTERNET:
- www.saludpublica.com: Tratamiento de la parálisis cerebral infantil con toxina botulínica .
- www.dolor-pain.com: Espasticidad
- www.revneurol.org: Experiencia del tratamiento con toxina botulínica en la espasticidad
- www.meodysoft.com: Toxina botulínica en espasticidad
- www.abtusalub.com: Infiltración de la toxina botulínica en el espasmo hemifacial
- www.getm.net: Tratamiento con toxina botulínica en la espasticidad, tratamiento con toxina botulínica en los tics ...
- www.neuropediatria.org: Análisis de los pacientes con respuesta muy favorable al tratamiento de la espasticidad con toxina botulínica A
No hay comentarios:
Publicar un comentario